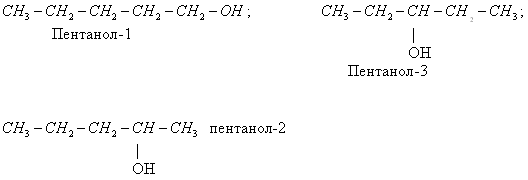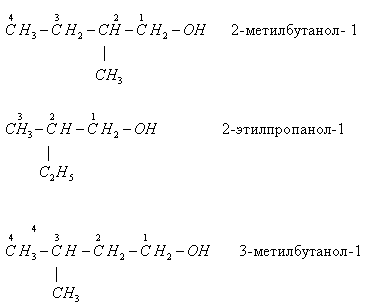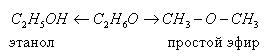Ізомерія
Поняття «ізомерія» ввів у хімію Й. Берцеліус в 1830 р., а справжнє обґрунтування було дано в 2 половині 19 століття.
Ізомерія — факт наявності химсоединений — ізомерів, що володіють ідентичною молекулярною масою і складом, але відмінних за місцезнаходженням або будовою атомів і за властивостями.
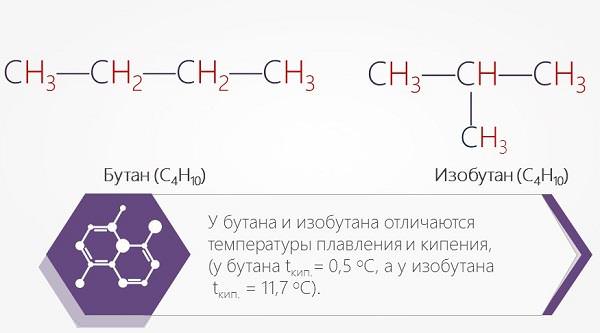
Так, формула бутану – С4Н10. Бутан, в молекулі якого вуглецеві атоми розташовуються у формі лінійної ланцюга, називають звичайним, а бутан, ланцюг атомів якого має розгалужену структуру, дають назву ізобутан.
Для граничних одноатомарных спиртів характерні три види ізомерії:
- ізомерія розташування функціональних груп і подвійного зв’язку:

- ізомерія вуглецевого скелета:

- міжкласова:

Номенклатура
Як утворюється назва спирту?
Найменування спирту = найменування вуглеводню + префікс + -ОЛ + (n1, n2…, nn), що означає кількість гідроксил в молекулі: 2 – «ді», 3 – «три», 4 – «тетра» і т. д.
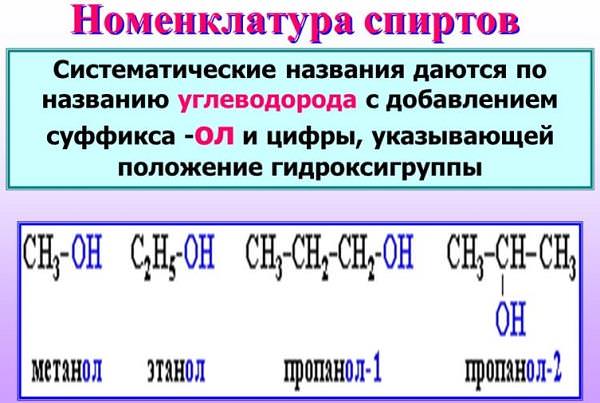
Присвоювання номери атомів вуглецю починається з закінчення, найближчого до гидроксогруппе.
Буква n повідомляє розташування гидроксогрупп в ланцюжку вуглеців.
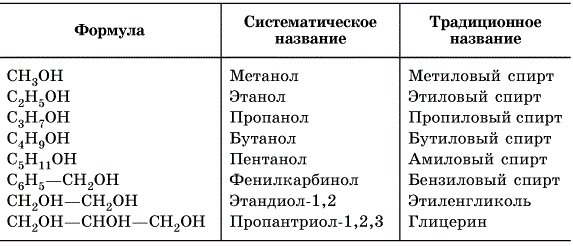
Насичені одноатомарные спирти утворюють гомологічний ряд. Структурна формула алканолов: c n h 2n +1 OH. Відкриває ряд метанол CH3OH. Далі йде етанол C2H5OH. Потім – пропанол C3H7OH, бутанол C4H9OH і т. д.