Хімічні властивості спиртів це їх реакції при взаємодії з іншими сполуками, обумовлені гидроксилами.
Вони майже нейтральні: не змінюють колір індикаторів, не реагують ні з розведеними кислотами, ні з лужними та водними розчинами.
Але в певних реакціях демонструють властивості дуже слабких основ і кислот.
Класифікація спиртів
Атомность визначається так:
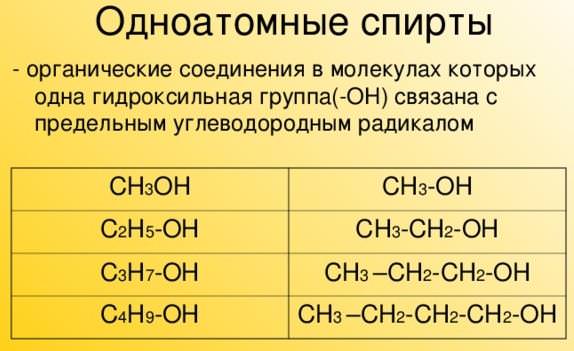
- В молекулі одноатомного спирту є одна гидроксогруппа: СН3 – СН2 – СН2ОН (пропанол С3Н7ОН).

- В молекулі багатоатомного спирту є дві або більше гидроксилы: СН2ОН — СН2 — СН2ОН.

Спирти класифікуються за трьома характеристиками:
- Кількість гідроксилов:
- одноатомні (етанол С₂Н₅ОН, СН₃СН₂ОН);
- двоатомні (етиленгліколь C₂H₆O₂, C₂H₄(OH)₂);
- багатоатомні (гліцерол C3H5(OH)3);
- Характер вуглеводневого радикалу:
- ненасичені похідні ненасичених вуглеводнів, атом водню в молекулах яких заміщується на гидроксогруппу: алліловий спирт Н2С = СН — СН2 — ОН;
- граничні — похідні насичених вуглеводнів, у яких один або більше водневих атомів заміщуються на гидроксогруппу. Формула: R — ВІН, де R — радикал: CH3 — CH2 — OH (етанол);
- ароматичні включають OH в бічній ланцюгом (бензиловий спирт);
- Характер атома вуглецю, що має зв’язок з гидроксогруппой:
- первинні — гидроксогруппа розташована у атома вуглецю, що має зв’язок лише з ще одним його атомом (приклад: R — CH2 — OH (етанол));
- вторинні — гидроксоруппа розташований у атома вуглецю, який пов’язаний лише з двома сусідніми його атомами (приклад: R — СН(ОН) — R’ (пропанол – 2));
- третинні — гидроксогруппа розташована у атома вуглецю, пов’язаного з трьома сусідніми його атомами (приклад: R — C — OH (2-метілпропанол-2)).