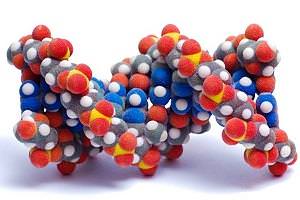
Будова білків
Беки відносяться до лінійних полімерів. У їх складі можуть бути присутні кілька α-амиокислот і неаминокислотные компоненти. На перший погляд всього 20 амінокислот – це невеликий вибір.

Але насправді молекула білка, яка складається всього з 5 компонентів амінокислот, може мати понад мільйон варіантів побудови. Невеликий білок може мати у своїй ланцюжку сотню амінокислотних залишків.
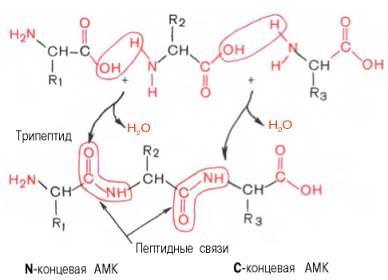
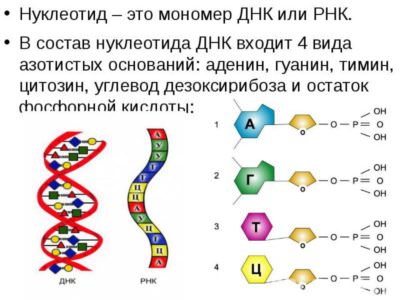
При синтезі білка амінокислоти з’єднуються завдяки пептидного зв’язку. Вони з’єднуються різними кінцями, одна з допомогою карбоксильної групи (-COOH), а інша аміногрупою (-NH2). При такому з’єднанні в білку з’являються два відповідних кінця С і N.
Структури білків
Структурні організації білків класифікують на 4 рівня. Це первинна, вторинна, третинна та четвертинна структури.
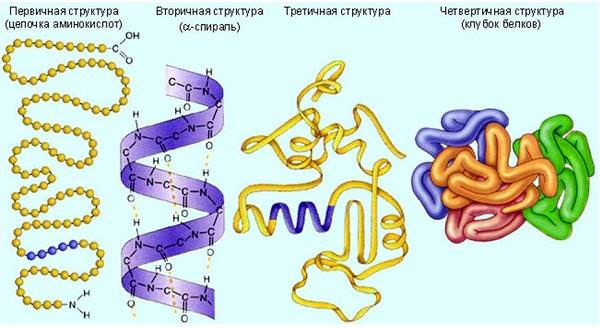
Первинна являє собою стандартну ланцюжок амінокислот. Їх послідовність генетично закодована. Вона зазвичай описується трехбуквенными позначеннями амінокислотних залишків в ланцюжку.
Вторинна являє собою впорядковано згорнуту спіралеподібно ланцюжок амінокислот. Вона нагадує пружинку. У спіралі стабільна структура, так як її витки кріпляться між собою водневими зв’язками. Майже все З – та NН – групи встановлюють один з одним такі зв’язки. Серед білків даної структури особливо виділяються колагени і кератин.
Третинна – в основному формується завдяки гідрофільно-гідрофобним взаємодіям. Виникають водневі іонні і дисульфідні зв’язки сприяють взаємодії між радикалами амінокислот. Завдяки цьому полипептидная зв’язок укладається в спеціальні глобули. До білків третинної структури відносяться безліч ферментів, антитіл і гормонів.
Четвертинна – притаманна складних форм ферментів або білків, які складаються з 2 або 3 глобул. Вони зв’язуються в молекулі як іонними, так і гідрофобними взаємодіями. А іноді виникають електростатичні взаємодії або дисульфідні зв’язки. Найбільш відомий і вивчений білок даної класифікації – гемоглобін.