Ізобарний процес і ΔU
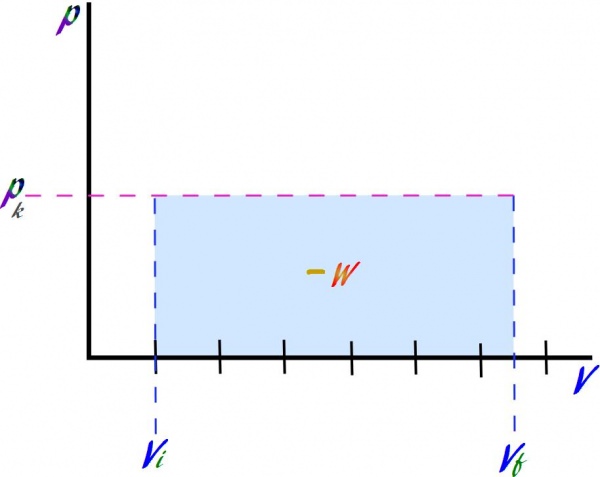
У разі изобарного процесу в системі підтримується постійний тиск. При цьому температура і об’єм змінюються в прямої пропорційності один щодо одного. Цей изопроцесс описується законом Шарля:
V / T = const при P = const.
У цьому випадку повідомлена системі енергія Q витрачається на роботу і зміну внутрішньої енергії, тобто:
ΔQ = A + ΔU = P * ΔV + z / 2 * n * R * T.
З урахуванням рівняння стану Клапейрона-Менделєєва можна записати такі формули для ΔU у разі изобарного переходу між станами ідеального газу:
ΔU = z / 2 * n * R * T = z / 2 * P * ΔV.
З цих рівностей випливає, що ККД одноатомного газу при изобарном розширенні вище, ніж ККД багатоатомного газу. Однак навіть для одноатомного газу більша частина енергії Q витрачається на збільшення внутрішньої енергії системи, ніж на вчинення нею роботи. Останній факт легко показати, якщо взяти відношення між величинами ΔU і A:
ΔU / A = 3 / 2 * P * ΔV / (P * ΔV) = 1,5.
ККД при изобарном розширенні одноатомного ідеального газу становить:
ККД = A / Q = P * ΔV / (3 / 2 * P * ΔV + P * ΔV) * 100% = 40%.








