Хімічні властивості
У звичайних умовах малоактивний. Причина — з’являється при дії кисню повітря оксидна плівка. Якщо ж порошок металу злегка нагріти, він згорає, перетворюючись в Mno 2.
При нагріванні взаємодіє з водою, витісняючи водень. В результаті реакції виходить практично нерозчинний гідрат закису Mn(OH)2. Це речовина перешкоджає подальшому взаємодії з водою.
Цікаво! Водень розчинний у марганці, і при підвищенні температури розчинність збільшується (виходить розчин газу в металі).
При дуже сильному нагріванні (температура вище 1200 градусів за шкалою Цельсія) взаємодіє з азотом, при цьому утворюються нітриди. Ці сполуки можуть мати різний склад, що типово для так званих бертоллидов. Взаємодіє з бором, фосфором, кремнієм, а в розплавленому вигляді — з вуглецем. Остання реакція протікає при відновленні марганцю коксом.
При взаємодії з розбавленою сірчаною і соляною кислотами виходить сіль і виділяється водень. А ось взаємодія з міцною сірчаною кислотою інше: продукти реакції — сіль, вода і двоокис сірки (спочатку сірчана кислота відновлюється в сірчисту; але з-за нестійкості сірчиста кислота розпадається на діоксид сірки і воду).
При реакції з розведеною азотної кислотою виходить нітрат, вода, окисел азоту.
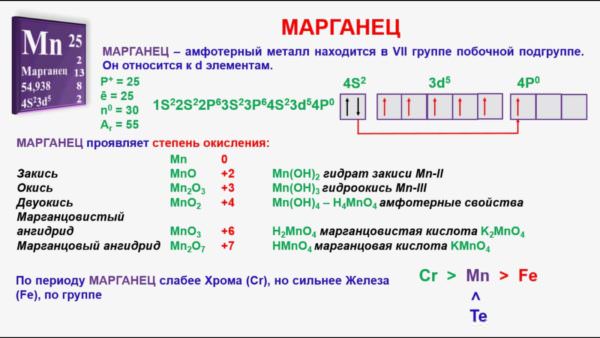
Утворює шість оксидів:
- закис, або MnO,
- окис, або Mn2O3,
- закис-окис mn 3 o 4,
- двоокис, або Mno 2,
- марганцеватый ангідрид MnO3,
- марганцевий ангідрид Mn2O7.
Цікаво! Закис під впливом кисню повітря поступово перетворюється в оксид. Ангідрид марганцеватой кислоти не виділяється в вільному вигляді.
Закис-окис — з’єднання з так званої дробової ступенем окислення. При розчиненні в кислотах утворюються солі двовалентного марганцю (солі з катіоном Mn3+ нестійкі і відновлюються до сполук з катіоном Mn2+).
Двоокис, окис, закис-окис — найбільш стійкі оксиди. Марганцевий ангідрид нестійкий. Простежуються аналогії з іншими хімічними елементами:
- Mn2O3 і mn 3 o 4 — основні оксиди, і по властивостях схожі на аналогічні сполуки заліза;
- Mno 2 — амфотерний оксид, за властивостями схожий на оксиди алюмінію і тривалентного хрому;
- Mn2O7 — кислотний оксид, за властивостями дуже схожий на вищий оксид хлору.
Нескладно помітити аналогію з хлоратами і перхлорату. Манганаты, подібно хлоратам, виходять непрямим шляхом. А ось перманганаты можна отримати як прямим шляхом, тобто при взаємодії ангідриду та оксиду/гідроксиду металу в присутності води, так і непрямим.
В аналітичній хімії катіони Mn2+ потрапив у п’яту аналітичну групу. Є кілька реакцій, що дозволяють виявити цей катіон:
- При взаємодії з сульфідом амонію випадає осад MnS, його колір — тілесний; при додаванні мінеральних кислот спостерігається розчинення осаду.
- При реакції з лугами виходить білий осад Mn(OH)2; однак при взаємодії з киснем повітря колір осаду змінюється з білого на буре — виходить Mn(OH)3.
- Якщо до солей з катіоном Mn2+ додати перекис водню розчин лугу, випадає темно-бурий осад MnO(OH)2.
- При додаванні до солей з катіоном Mn2+ окислювача (двоокис свинцю, висмутат натрію) і міцний розчин азотної кислоти, розчин забарвлюється в малиновий колір — це означає, що Mn2+ окислився до HMnO4.
Хімічні властивості








