Формули изохорной і изобарной теплоємностей повітря
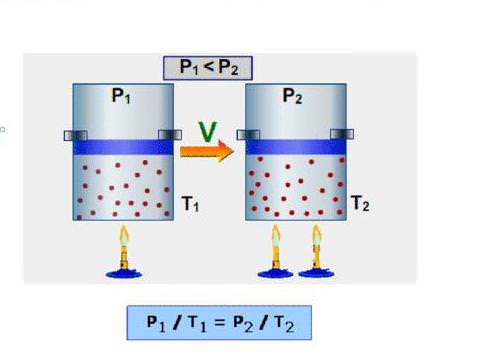
Спочатку розглянемо изохорную величину. Позначимо її CV. Перше початок термодинаміки, яке випливає з закону збереження енергії, для ізохорний процесу виглядає наступним чином:
H = dU
Тобто все тепло H, що підводиться до системи, йде на збільшення її внутрішньої енергії. Зміна величини U можна записати так:
dU = CV*dT
З іншого боку, якщо скористатися універсальним рівнянням стану ідеального газової системи, то формула для dU запишеться у вигляді:
dU = z/2*n*R*dT
Тут z – кількість ступенів свободи молекул, n – кількість речовини, R – постійна, dT – зміна температури. Вираз вище випливає з того факту, що внутрішня енергія ідеального газу в точності дорівнює кінетичної енергії його молекул.
З порівняння двох рівностей одержуємо формулу для изохорной теплоємності:
CV = z/2*n*R
У разі повітря z=5, оскільки він на 99 % складається з двоатомних молекул азоту і кисню (двохатомні молекули мають 3 поступальні і 2 обертальні ступені свободи). Вважаючи n=1 моль, приходимо до формули изохорной молярної теплоємності повітря:
CV = 5/2*R = 2,5*R
Нагадаємо, що постійна R дорівнює 8,314, тоді CV = 20,785 Дж/(моль*К).
Тепер визначимо молярную изобарную теплоємність повітря. Оскільки в результаті изобарного нагрівання газ розширюється, то він виконує певну роботу. Перше початок термодинаміки в цьому випадку приймає вигляд:
H = dU + P*dV
Ентальпія H через изобарную теплоємність CP для 1 моль речовини запишеться так:
H = CP*dT
Роботу газу з використанням рівняння Клапейрона-Менделєєва можна записати так:
P*dV = R*dT
Ці вирази дозволяють записати наступне співвідношення изобарной і изохорной теплоємностей:
CP = CV + R
Підставляючи величину CV для повітря, отримуємо изобарную молярную теплоємність для нього:
CP = 2,5*R + R = 3,5*R = 29,099 Дж/(моль*К)
Таким чином, величина CP виявляється більше, ніж CV.