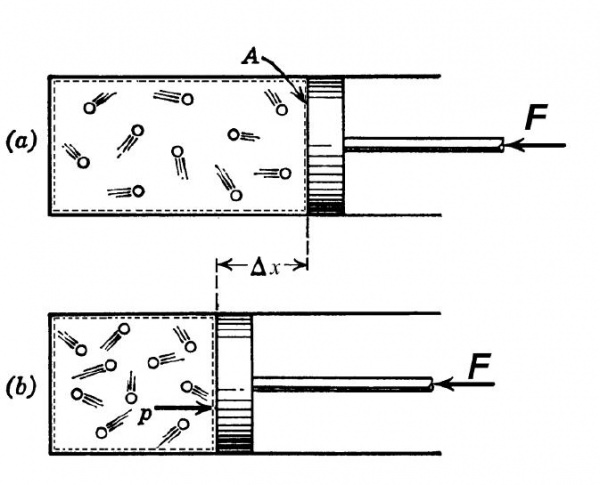
Фізичний сенс
Величина γ називається показником адіабати. Він математично дорівнює відношенню теплоємності СР і СV. Оскільки ізобарна теплоємність завжди більше изохорной, то γ буде більше 1. Чому це відбувається? У разі изобарного процесу підводиться до системи теплота витрачається не тільки на її нагрів, але й на здійснення системою роботи.
На показник адіабати не впливає хімічний склад газу, проте він залежить від кількості ступенів свободи, що складають систему молекул. У загальному випадку справедлива наступна формула:
γ = (f + 2) / f
Тут f – число ступенів свободи. Для одноатомного газу воно дорівнює 3, для двоатомних – 5, а для багатоатомного – 6. З урахуванням цих цифр отримуємо значення γ:
γ = 1,67 (для одноатомного);
γ = 1,4 (для двоатомних);
γ = 1,33 (для багатоатомного)
У разі газової суміші, в яку входять молекули з різним числом атомів, слід розраховувати середнє значення γ з урахуванням атомних часток компонентів. Наприклад, земне повітря на 99 % складається з двоатомних молекул N2 та O2, тобто для нього показник γ для стандартних умов практично дорівнює 1,4.