Калієва сіль хлорноватої кислоти, або хлорат калію, являє собою неорганічні з’єднання, що володіє вибуховими властивостями. Висока чутливість до тертя і реакційна здатність обмежують область його застосування в промисловості.
Загальний опис
Хлорат калію – тверда речовина у вигляді дрібного кристалічного порошку білого кольору, не має запаху. Кристали мають пластинчастої, голчастої або призматичної форми. Інша назва цього з’єднання – бертолетова сіль. Воно присвоєно по імені французького хіміка Клода Луї Бертолле. Цей вчений вперше синтезував дана речовина в 1786 році за допомогою пропускання хлору через розчин калієвого лугу. Тоді ж були відкриті і його вибухові властивості.
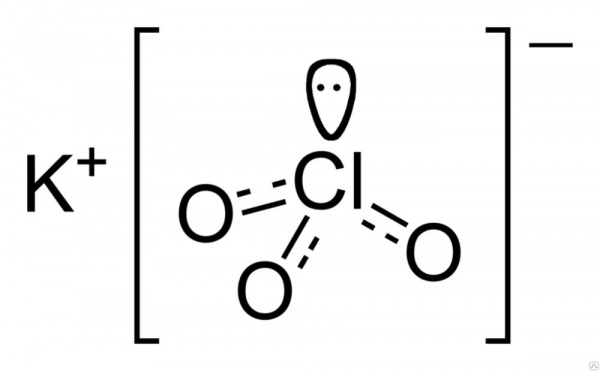
Емпірична формула хлорату калію має вигляд: ClKO₃.
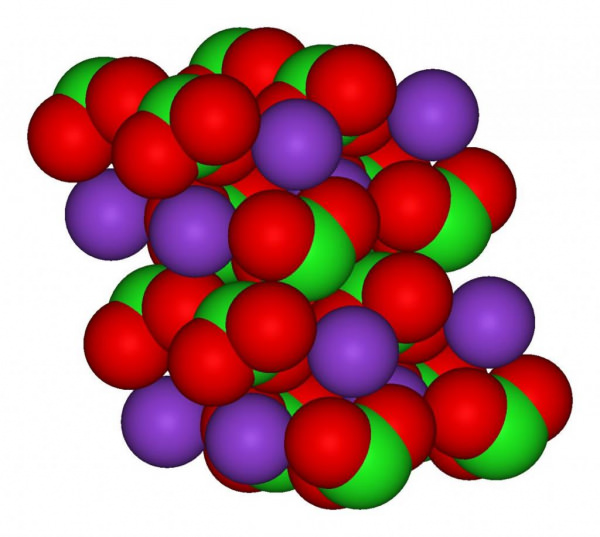
Структурно речовина представлено на малюнку нижче. Три атома кисню пов’язані з атомом хлору допомогою ковалентного зв’язку, а взаємодія атома калію і хлору носить іонний характер.
За хімічним складом компоненти розподіляються таким чином:
- К – 31,92 %;
- Cl – 28,92 %;
- Про – 39,16 %.








