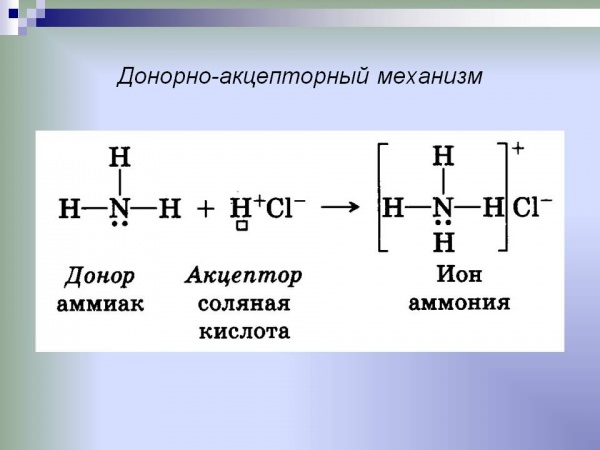
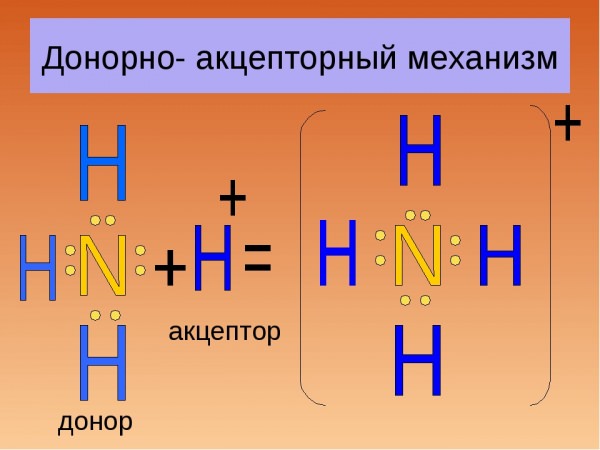
Утворення чадного газу
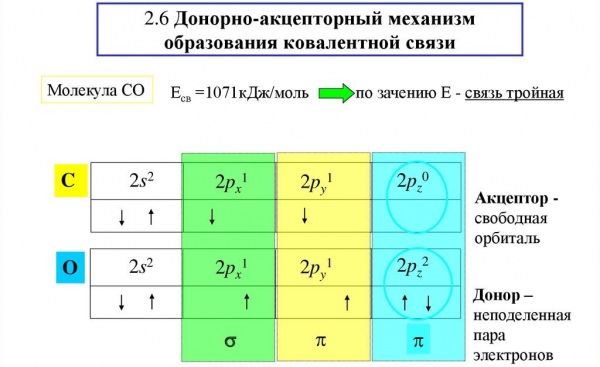
Донорно-акцепторний механізм можна розглянути на прикладі молекули СО. У атома вуглецю на зовнішньому енергетичному рівні розташовуються два неспарених електрона. Таку ж кількість неспарених електронів є і у атома кисню. В результаті між атомами утворюється подвійний зв’язок.
За рахунок пари електронів кисню і порожній орбіталі вуглецю, для одержання зв’язку використовується донорно-акцепторний механізм.
Молекула азотної кислоти
Завдяки наявності трьох неспарених електронів атом азоту в даному з’єднанні утворює три варіанти зв’язків: з киснем подвійну, одинарну з киснем гідроксильної групи. За донорно-акцепторної механізму утворена зв’язок між ще одним атомом кисню і азоту.
Неспарені електрони розміщуються на одній орбіталі, при цьому одна звільняється.
Також можна припустити, що атомом азоту відданий кисню електрон. Перетворившись на катіон амонію, має 4 неспарені електрони, він утримує аніон завдяки сил електростатичної взаємодії.