Принцип невизначеності Гейзенберга: область всередині атома
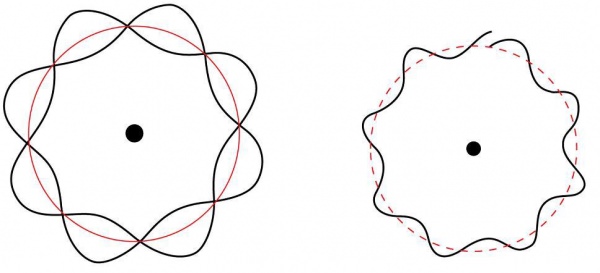
Луї де Бройль запропонував, щоб всі частинки можна було розглядати, як матеріальні хвилі з довжиною хвилі лямбда, визначається наступним рівнянням:
Лямбда = фактичний час (год) + милливольтчас
Ервін Шредінгер запропонував квантово-механічну модель атома. Коротко: вона розглядає електрони, як хвилі речовини.
Квадрат хвильової функції є ймовірність знаходження електрона в даній області всередині атома. Атомна орбіта визначається, як область всередині атома, що знаходиться там, де електрон.
Принцип невизначеності Гейзенберга говорить, що ми не можемо знати енергію, ні положення електрона. Тому, коли ми більше дізнаємося про стан електрона, ми менше знаємо про його енергії, і навпаки. Електрони мають внутрішнє властивість, зване спіном. Будь-які два електрона, займають одну і ту ж орбіту, повинні мати протилежні спини.








