Винна кислота належить до класу карбонових кислот. Свою назву ця речовина отримала з-за того, що основним джерелом його одержання служить виноградний сік. При бродінні останнього відбувається виділення кислоти у вигляді погано розчинної калієвої солі. Основною областю застосування цієї речовини є виробництво продукції харчової промисловості.
Загальний опис
Винна кислота відноситься до категорії ациклічних двоосновний гидрокислот, у складі яких міститься і гидроксильная, та карбоксильна групи. Такі сполуки розглядають також як гідроксильні похідні карбонових кислот. Ця речовина має й інші назви:
- диоксиянтарная;
- тартаровая;
- 2, 3-дигидроксибутандиовая кислота.
Хімічна формула винної кислоти: С4Н6О6.
Для даного з’єднання характерна стереоизометрия, воно може існувати в 3 формах. Структурні формули винних кислот представлені на малюнку нижче.
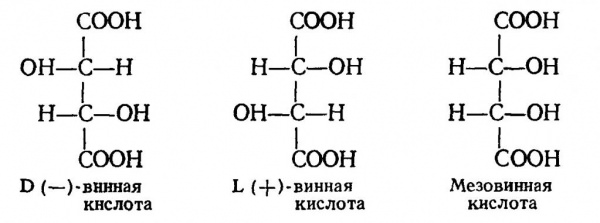
Найбільш стійкою є третя форма (мезовинная кислота). D – і L – кислоти – оптично активні, але суміш цих ізомерів, взятих в еквівалентній кількості, оптично неактивна. Таку кислоту ще називають r – або i-винною (рацемической, виноградної). За зовнішнім виглядом дана речовина – це безбарвні кристали або білий порошок.








