Відомо три агрегатних стани речовини, і одне з них – газоподібний. Газів існує багато. Постійно відкриваються нові. У цій статті ви дізнаєтеся про самих важких газах.
Але що значить важкий? Ніхто не набирав в колбу газ і не зважував на терезах. Тим більше, деяких летких речовин на всій планеті не набереться і півлітра.
«Важкість» речовини визначається молекулярною масою – приблизною масою всіх його молекул. Однак саме число мало що розповість про речовині. Наочніше порівняти з повітрям. Якщо поділити відносну молекулярну масу на 29, ми дізнаємося, наскільки цей газ важчий за повітря.
Варто обмовитися. Цей список – не самий достовірний, адже щодня синтезується безліч газів. Неможливо порівняти все, що створила людина. Тут описані відомі речовини, але напевно є інертні гази, важчі представлених.
10. Perfluorotrimethylamine (N(CF3)3)
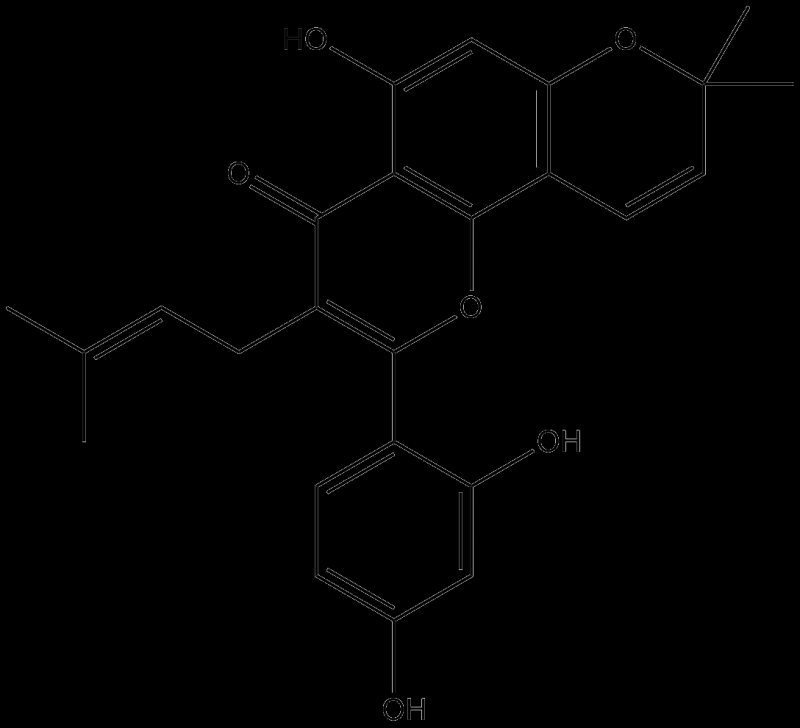
Якщо взяти аміак NH4 і замінити на водні метилові радикали –CH3, також замінивши в них водень фтором, вийде перфтортриметиламин.
N(CF3)3 кипить при -6С. Тобто, якщо винести колбу з рідиною на вулицю, то вже при -6 градусів вона почне кипіти і випаровуватися. Відносна молекулярна маса газу – 221. Поділимо на 29 і дізнаємося, що perfluorotrimethylamine важче повітря в 7,6 разів.
9. Радон (Rn)

Радон, на відміну від інших у списку, не синтезований людиною. Це хімічний елемент, що займає 86 позицію в таблиці Менделєєва. Радон — майже не вступає в реакції радіоактивний газ.
Період напіврозпаду — 4 дні. Тобто, якщо взяти ємність з радоном і поставити в кімнату, через чотири дні в колбі залишиться половина взятого газу. Інша частина розпадеться на більш легкі елементи. Та й сам радон – продукт радіоактивного розпаду елемента радію. Так що не варто проробляти цей досвід, нехай він залишиться уявним.
Радіоактивний радон присутній скрізь: у школах, на вулицях, у повітрі, ґрунті і навіть у воді. На уроках фізики проводять практичну роботу. Учні спускаються в підвал і вимірюють рівень радіації. Але чому в підвал?
Це пов’язано з тим, що радон – важкий газ. Відносна молекулярна маса – 222. Поділивши на 29, з’ясовуємо, що він важчий за повітря в приблизно в 7-8 разів. Оскільки більш тяжкий речовина опускається вниз, найбільше радону знаходиться внизу, в підвалах і шахтах. Однак середній рівень радіації в повітрі невеликий, так що не бійтеся тепер спускатися в підвали.
8. Perfluorobutane (C4F10)

Перфторбутан – це звичайний бутан C4H10, в якому атоми водню змінили на фтор.
C4F10 – малоактивне речовина. Воно неохоче вступає в реакції, а тому не являє загрози організму. На нього не діють навіть кращі окислювачі – азотна і сірчані кислоти.
Перфторбутан знайшов різноманітне застосування. Пожежники використовують газ як наповнювач для вогнегасників, лікарі – як контрастну речовину для УЗД, для інженерів це холодильний агент.
Молекулярна маса газу – 238 а.е.м. Таким чином, речовина, важча за повітря у 8,2 рази.
7. Tellurium hexafluoride (TeF6)
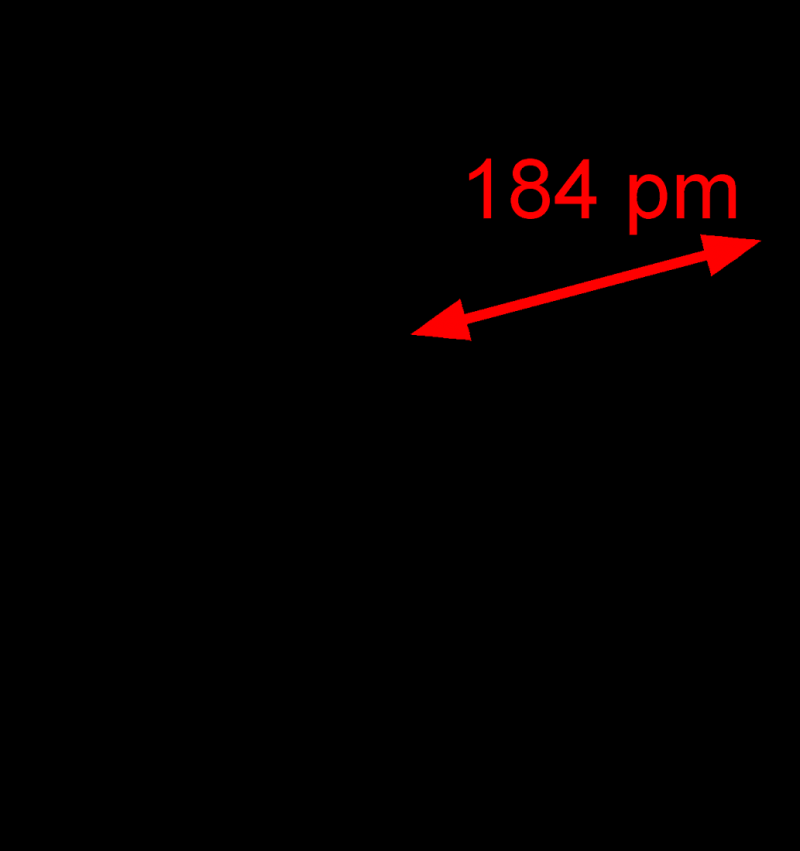
Телур, обвішаний фтором, як новорічна ялинка – це TeF6. Як і у більшості газоподібних сполук телуру, у гексафториду вкрай неприємний запах. Але це ще півбіди. Безбарвний газ дуже токсичний і небезпечний для здоров’я. Також реагує з водою, розкладаючись в ній і утворюючи нові сполуки.
Молекула важить приблизно 241,6 а.е.м., а тому важче повітря у 8,33 рази.
Можливо, ви вже помітили, що у складі важких газів постійно виникає фтор. Але ж є елементи важче фтору, чому б не замінити водні на них? Справа в тому, що фтор – найбільш «агресивний» елемент. Атому не вистачає всього одного електрона для досягнення балансу. Так що він з задоволенням відбирає електрони у інших елементів. В молекулі легше замінити легкий водень на більш важкий фтор – він активно вступає в реакції і обважнює молекулу.
6. Перфторэтил йодид (CF3CF2I)
Речовина походить від йодэтана – безбарвної рідини, желтеющей на повітрі із-за присутності йоду. Йодэтан може бути канцерогеном, тобто викликати злоякісні пухлини. Також з’єднання володіє слабким наркотичним ефектом.
CF3CF2I – це йодэтан, в якому водень знову замінили на фтор. Разом із зміною складу змінюються і властивості речовини. Так, повідомляють, що газ використовують для анестезії. Значить, він вже не такий шкідливий, як йодэтан.
Маса перфторэтид йодиду – 245,9, речовина, важча за повітря у 8,5 разів.
5. Decafluorodiethyl ether (C4F10O)
Діетиловий ефір C4H10 отримали ще в IX столітті, після чого відкривали ще три рази. Великий хірург Н.І. Пирогов вперше став використовувати діетиловий ефір для знеболювання під час операцій. З тих пір речовина прийняли як засіб анестезії.
Замінивши водні на фтор, люди отримали C4F10O . Швидше за все, даний ефір теж придатний для наркозу. Але цього ніхто не перевіряв. Відносна молекулярна маса – 254, газ важче повітря в 8,8 разів.
4. Tellurium hypofluorite (F5TeOF)

Маса F5TeOF – 259,6 а.е.м., важчий за повітря в 9 разів. Кипить при температурі +0,6 С. Відповідно, при більш низькій температурі – це рідина. Судячи з того, що гипофторит – з’єднання теллура, цей газ теж токсичний і неприємно пахне.
3. Iodine heptafluoride (IF7)
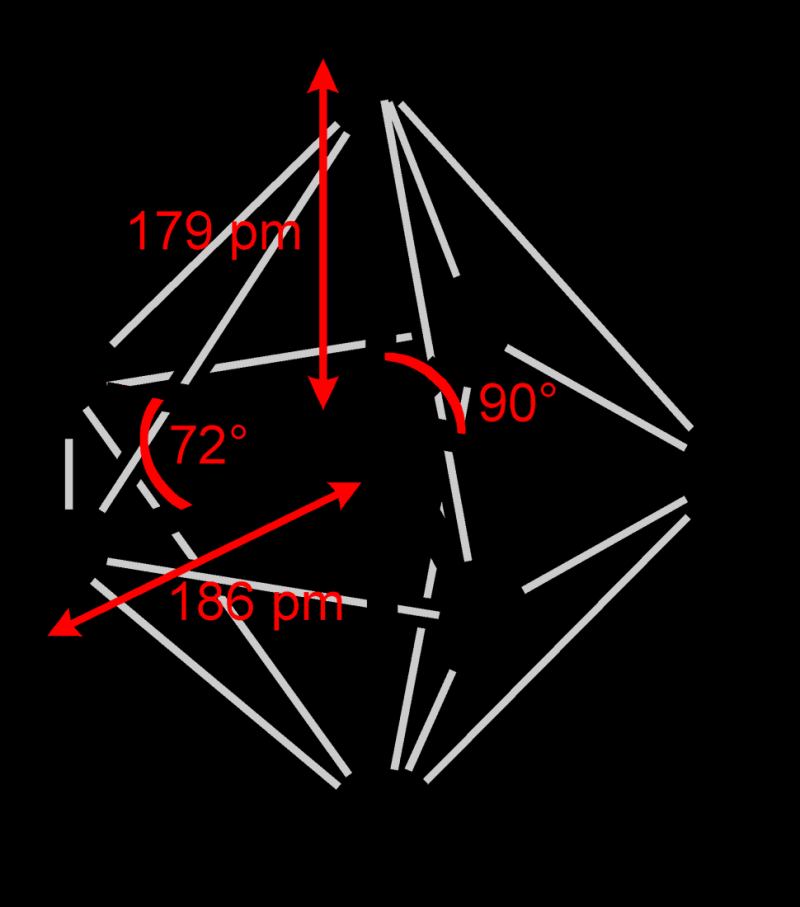
IF7 – безбарвний газ з різким запахом, вищий фторид йоду. Обидва елемента I і F повністю заповнили електронні оболонки. Досягли «ідеального балансу», до якого прагнуть всі хімічні елементи.
Дивлячись на формулу, хочеться додати у з’єднання хлор і отримати ще більш важку молекулу IClF6. Однак на практиці цього не виходить. Так вже виходить, що немає сполук, в яких присутній більше двох видів галогенів.
Гептафторид йоду – надзвичайно активна речовина. Це сильний окислювач, він з радістю «нападає» на метали, а в контакті з органікою викликає пожежа. З-за такої активності IF7 небезпечний для організму людини. З’єднання сильно подразнює слизові оболонки.
Газ важче повітря майже в 9 разів, молекулярна маса – 259,6 (як і у минулого речовини зі списку).
2. Hexamethyltungsten (W(CH3)6)
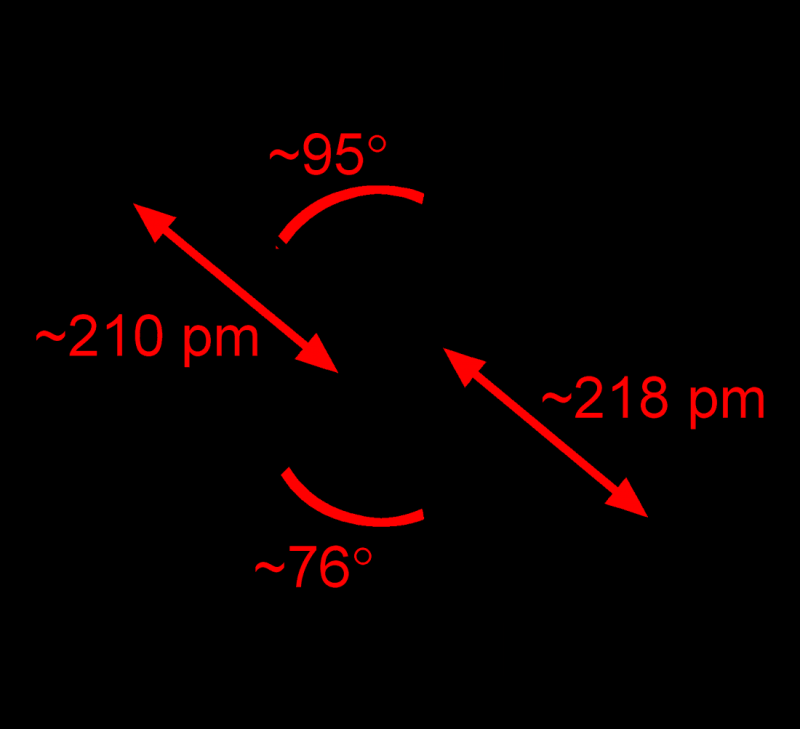
Якщо атом вольфраму, з якого роблять лампи розжарювання, з усіх сторін «обліпити» метиловим радикалами –CH3, вийде гексаметилвольфрам.
З’єднання вибухонебезпечно на повітрі і у вакуумі. І взагалі дуже нестійкий. W(CH3)6 виявилося в цьому списку з натяжкою, адже речовина розпадається майже відразу після освіти. Молекула важить 274,05 а.е.м, а тому важче повітря в 9,45 раз.
1. Tungsten hexafluoride (WF6)
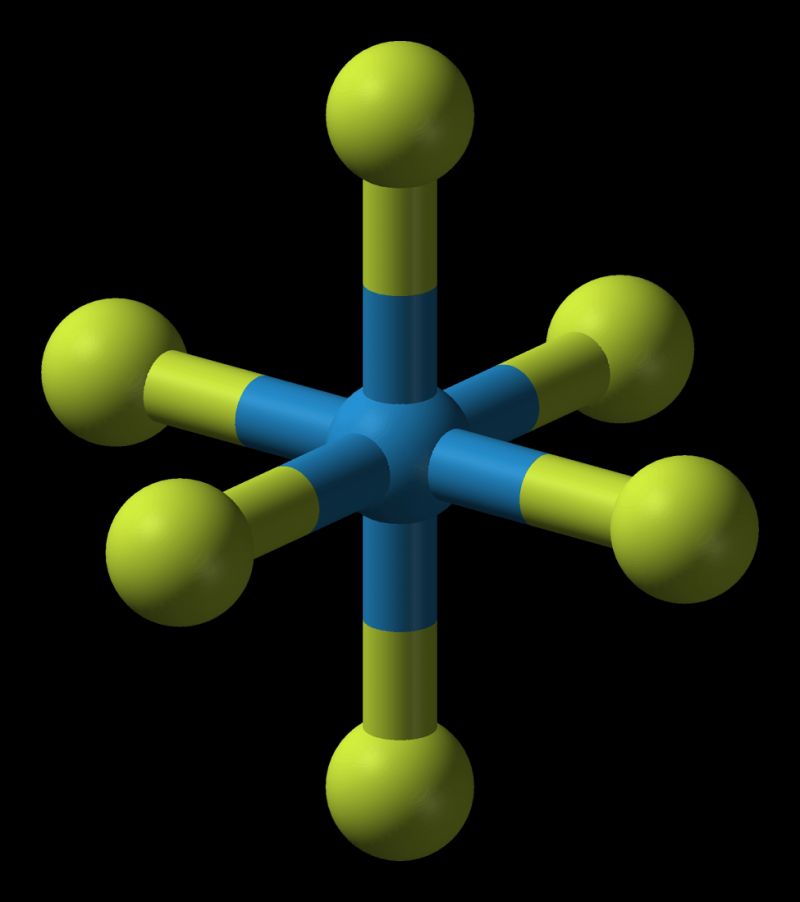
Самий важкий газ в топі – WF6, гексафторид вольфраму. Це сіль плавикової кислоти HF і вольфраму W. Речовина газообразно при температурі вище +17 С, так що знаходиться на межі з рідиною. У вологому повітрі починає диміти і синіти.
WF6 – корозійно активне з’єднання, а також найнебезпечніший неорганічний отрута. Тим не менш, газ застосовують у виробництві напівпровідників і вольфрамових покриттів.
Відносна молекулярна маса tungsten hexafluoride – 297.3. Газ важче повітря більше ніж у 10 разів. WF6 стає рекордсменом серед найбільш важких газів.