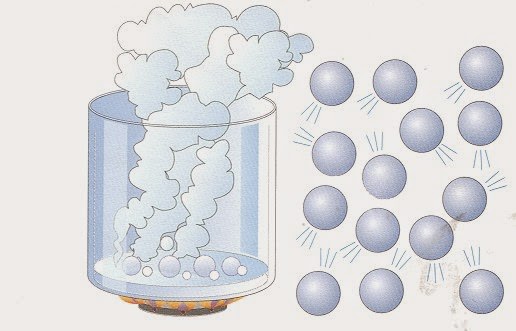
У фізиці рідких субстанцій велика увага приділяється вивченню газів, яке здійснюють за допомогою використання моделі ідеального газу. У цій області було відкрито багато законів. У наведеній нижче статті вивчимо формулу концентрації молекул газу (ідеального) і покажемо, як її слід застосовувати при вирішенні практичної проблеми.
Ідеальний газ
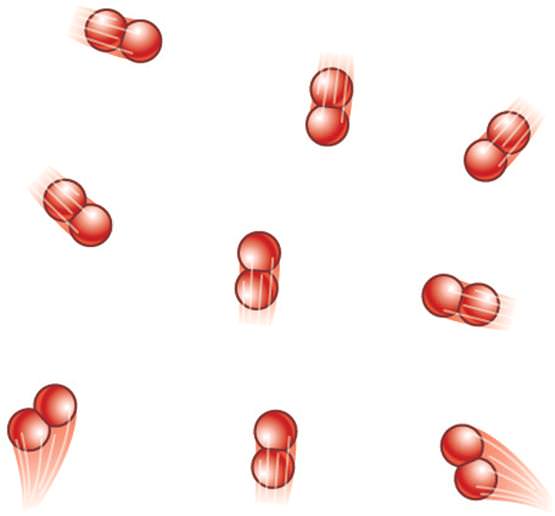
Що ж це таке? Перш ніж записати формулу концентрації молекул газу, розповімо, що являє собою модель ідеального газу. Згідно з кінетичною теорією сипучих субстанцій, в таких речовинах молекули та атоми рухаються хаотично з прямим траєкторіях. Відстані між ними набагато більше, ніж їхні власні лінійні розміри, тому останніми нехтують при виконанні обчислень. Крім того, вважають, що взаємодій між молекулами не існує, оскільки їх кінетична енергія дуже велика в порівнянні зі слабкими потенційними взаємодіями.
Будь-які реальні гази, які знаходяться при низьких тисках і досить високих абсолютних температурах, за своєю поведінкою наближаються до описаної моделі. Тим не менше, існують текучі субстанції, у яких крім ван-дер-ваальсових взаємодій між частинками діють взаємодії більш сильного характеру. Прикладом є водяна пара, у якої молекули друг з одним пов’язані водневими (полярними) зв’язками. Для опису поведінки таких субстанцій не можна використовувати модель ідеального газу.